تکنیک کروماتوگرافی | چیستی، اصول، فرآیند و انواع
تفکیک اجزای مختلف یک مخلوط یکی از نیازهای اساسی در علم شیمی و بیوشیمی به شمار میرود. کروماتوگرافی، یک اصطلاح جامع برای مجموعهای از تکنیکهای آزمایشگاهی است که بهمنظور جداسازی مخلوطها بهکار میروند. این روشها بر پایه عبور مخلوط حل شده در یک فاز متحرک از یک فاز ثابت عمل میکنند که این فرآیند باعث جداسازی جز مورد نظر از سایر مولکولهای موجود در مخلوط میشود. در ادامه با مجله بیوزوم همراه باشید تا بیشتر با تکنیک کروماتوگرافی و انواع آن آشنا شویم.
تکنیک کروماتوگرافی یک روش تحلیلی است که برای جداسازی مخلوطی از مواد شیمیایی به اجزای جداگانهاش استفاده میشود تا بتوان این اجزا را به طور کامل تجزیهوتحلیل کرد. انواع مختلفی از کروماتوگرافی از جمله کروماتوگرافی مایع، کروماتوگرافی گازی، کروماتوگرافی تبادل یونی و کروماتوگرافی میل ترکیبی وجود دارد. با وجود تفاوتهای بین این روشها، همگی از اصول اولیه یکسانی پیروی میکنند.
تکنیک کروماتوگرافی یک روش جداسازی است که هر شیمیدان آلی و بیوشیمیستی با آن آشنایی دارد. برای توضیح ساده این تکنیک، فرض کنید دو واکنشدهنده “A” و “B” وجود دارند که تحت شرایط خاص با یکدیگر واکنش داده و محصول “C” را تشکیل میدهند. پس از کاملشدن واکنش، مخلوطی از واکنشدهندههای A و B که واکنش ندادهاند و محصول موردنظر یعنی C باقی میماند.
در این مرحله، برای تجزیهوتحلیل محصول خالص C، نیاز به جداسازی A، B و C داریم. تکنیک کروماتوگرافی با استفاده از اصول جداسازی، این کار را به طور مؤثر انجام میدهد.
A+B→C
روند کلی تکنیک کروماتوگرافی
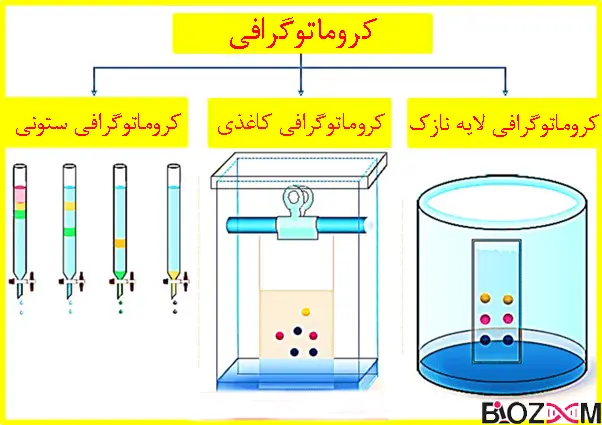
ابتدا، صفحه کروماتوگرافی لایهنازک (TLC) قابلاجرا است. این تکنیک اساساً شامل یک قطعه شیشهای مستطیلی است که با یک لایهنازک سیلیس پوشانده شده است.
یک نقطه از مخلوط واکنش درست بالای پایه صفحه (که با یک خط ثابت مشخص میشود) اعمال شده و صفحه در شیشهای قرار گرفته که حاوی حلال آلی مناسب با حجم کافی برای فرو بردن لبه پایینی صفحه است.
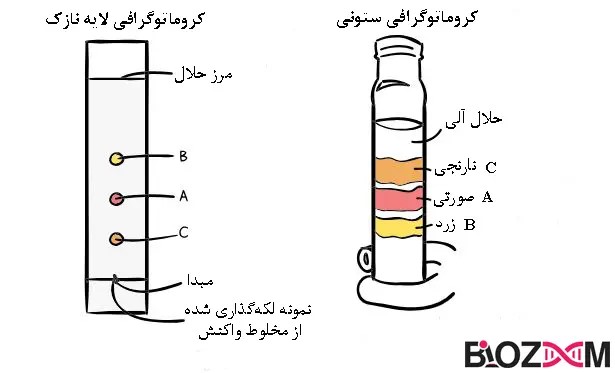
بهتدریج با عمل مویینگی، حلال شروع به بالارفتن از صفحه سیلیکا کرده و مخلوط واکنش تا زمانی که حلال به علامت جلویی حلال برسد به 3 نقطه با رنگهای متمایز جدا میشود.
در مرحله بعد، برای انجام عمل جداسازی، یک ستون شیشهای با یک دریچه در پایین آن مونتاژ میشود. یک پلاگین پنبهای در پایین ستون قرار داده شده و ستون با ژل سیلیکا (تهیه شده در یک حلال آلی) پر میشود. پس از بستهشدن ستون و کاهش حجم حلال بالای بستر به کمتر از 5 میلیمتر، مخلوط واکنش با دقت روی بستر سیلیس از بالای ستون با کمک یک پیپت شیشهای ریخته میشود.
حلال به آرامی از ستون عبور کرده و به طور مداوم از بالای ستون شیشهای اضافه میشود. مخلوط واکنش شروع به جدا شدن به سه نوار متمایز زرد، صورتی و نارنجی میکند که به ترتیب مربوط به B واکنش نداده، A بدون واکنش و محصول مورد نظر C است. نوارهای جداگانه در فلاسکهای جداگانه جمعآوری میشوند و در نتیجه، C خالص به دست میآید.
در بخشهای بعد بیشتر با تکنیک کروماتوگرافی لایه نازک و ستونی آشنا خواهیم شد.
در ادامه با اصول تکنیک کروماتوگرافی و اصطلاحاتی که در این تکنیک مورد استفاده قرار میگیرند بیشتر آشنا خواهیم شد:
اصول کروماتوگرافی
- فاز متحرک (Mobile Phase): حلال متحرک در ستون کروماتوگرافی است.
- فاز ساکن (Stationary Phase): مادهای است که در ستون، ثابت میماند.
- شوینده (Eluent): مادهای است که وارد ستون کروماتوگرافی میشود.
- محصول شویش (Eluate): مادهای است که در بالون جمعآوری میشود.
- شویش (Elution): شستشوی ترکیب از طریق ستون کروماتوگرافی با کمک یک حلال مناسب است.
- آنالیت (Analyte): مخلوط مورد مطالعه یا مخلوطی است که اجزای آن باید جداسازی شوند.
آنالیت در بالای یک بستر سیلیسی قرار گرفته و به آن زمان داده میشود تا به سیلیس (سیلیکا) بچسبد. در اینجا، سیلیکا بهعنوان فاز ساکن ایفای نقش میکند. سپس فاز متحرک یا حلال به کمک نیروی جاذبه یا فشار، از میان بستر سیلیسی وادار به حرکت میگردد. اجزای سازنده آنالیت، درجات مختلفی از چسبندگی به سیلیکا را از خود نشان میدهند.
در ادامه، این اجزای سازنده با سرعتهای متفاوتی از میان فاز ساکن عبور کرده و هنگام عبور، از یکدیگر جدا میشوند که این جداشدگی بهصورت نوارهای مختلف رنگی از یکدیگر قابلتشخیص هستند. جزئی که با شدت بالا به بستر جذب شده، سرعت حرکت کمتری در مقابل دیگر اجزا خواهد داشت.
آزمایشی با کروماتوگرافی
در ادامه توضیحات آزمایشی داده شده تا قدرت تکنیک کروماتوگرافی بهتر نشان داده شود.
در مرحله اول مقداری برگ جمعآوریشده و در ظرفی خرد میشود. یک قطره از عصاره برگ در حدود نیم سانتیمتر بالاتر از لبه کاغذ کروماتوگرافی، روی آن ریخته میشود.
نوار کاغذی در شیشهای حاوی استون قرار میگیرد. مقدار استون بهگونهای است که لبه پایینی کاغذ به خوبی در آن غوطهور میشود. برای جلوگیری از تبخیر محلول، روی ظرف پوشانده میشود.
سپس محلول به کمک نیروی مویینگی از داخل کاغذ به سمت بالا حرکت میکند. زمانی که حلال به نقطه انتهایی خود رسید، از داخل شیشه خارج میشود و اجزای مختلف تشکیلدهنده رنگِ برگ از یکدیگر جدا خواهند شد.
اصول جداسازی ترکیبات مختلف
دلیل جدایش اجزای مختلف آنالیت از یکدیگر، قدرت چسبندگی این اجزا در عبور از فاز ساکن است. میل ترکیبی (Affinity)، با دو خاصیت مولکول شامل جذب (Adsorption) و انحلالپذیری (Solubility)، تعیین میگردد.
جذب
به نحوه چسبندگی اجزای مختلف یک مخلوط به فاز ساکن اشاره دارد. هرچه جذبشدگی به فاز ساکن بیشتر باشد، حرکت مولکولها در ستون کروماتوگرافی آهستهتر خواهد بود.
انحلالپذیری
مربوط به انحلال اجزا در فاز متحرک است. هرچه انحلالپذیری در فاز متحرک بیشتر باشد، حرکت مولکولها در ستون سریعتر خواهد بود.
در نتیجه، برهمکنشهای بالا مشخص خواهند کرد که هر جزء آنالیت، با چه سرعتی در ستون حرکت کند. جذب و انحلالپذیری یک مولکول با انتخاب صحیح فاز متحرک و ساکن، قابلتغییر است.
در ادامه به این پرسش که چرا ترکیبات مختلف، میل ترکیبی متفاوتی دررابطهبا فاز متحرک و ساکن دارند، پاسخ میدهیم.
قطبیت
یک ترکیب، این حالت را تعیین میکند. فرض کنید مخلوطی از دو مولکول A و B وجود دارد. مولکول A پروتئین و مولکول B لیپید بوده و ستون کروماتوگرافی نیز شامل سیلیس است که در طبیعت خاصیتی قطبی دارد و فاز متحرک نیز هگزان و ناقطبی است.
اگر این ترکیب در ستون کروماتوگرافی وارد شود، مولکول A قطبی، جذب فاز ساکن قطبی خواهد شد. مولکول B هم بهسادگی در فاز متحرک ناقطبی حل شده و به سیلیس نمیچسبد، در نتیجه به همراه هگزان، از محلول شسته خواهد شد. هنگامی که B خارج شد، فاز متحرک به یک فاز قطبی مانند استونیتریل (Acetonitrile) تغییر میکند. با انجام این کار، مولکول A از سیلیس جدا شده و در حلال قطبی حل میشود. در نتیجه، مولکول A، به همراه استونیتریل از ستون شسته میشود.
تکنیکهای شکل تخت کروماتوگرافی (Techniques by chromatographic bed shape)
تکنیک کروماتوگرافی ستونی (Column chromatography)
تکنیک کروماتوگرافی ستونی یک تکنیک جداسازی است که در آن بستر ثابت درون یک لوله قرار دارد. ذرات فاز ثابت جامد یا تکیهگاه پوشش داده شده با فاز ساکن مایع ممکن است کل حجم داخلی لوله (ستون بسته) را پر کنند. همچنین، این ذرات ممکن است روی دیواره لوله داخلی یا در امتداد آن متمرکز شوند. در این صورت، یک مسیر باز و نامحدود برای فاز متحرک در قسمت میانی لوله (ستون لولهای باز) فراهم میشود. تفاوت در سرعت حرکت در محیط باتوجهبه زمانهای نگهداری مختلف نمونه قابلمحاسبه است.
در سال 1978، یک نسخه اصلاح شده از تکنیک کروماتوگرافی ستونی به نام کروماتوگرافی ستونی فلش(Flash Column Chromatography) معرفی شد. این تکنیک بسیار شبیه به کروماتوگرافی ستونی سنتی است، با این تفاوت که حلال با اعمال فشار مثبت در ستون رانده میشود. این کار اجازه می دهد تا اکثر جداسازیها در کمتر از 20 دقیقه، بهصورت جداسازی بهبود یافته در مقایسه با روش سنتی، انجام شود.
سیستمهای تکنیک کروماتوگرافی فلش مدرن بهعنوان کارتریجهای پلاستیکی از پیش بستهبندی شده فروخته شده و حلال از طریق کارتریج پمپ میشود. سیستمها ممکن است به آشکارسازها و جمعآوریکنندههای جزء متصل شوند و اتوماسیون را فراهم کنند.
جذب بستر توسعهیافته (Expanded Bed Adsorption) برای جداسازی و تصفیه مولکولها از مخلوطهای پیچیده استفاده میشود. در این روش، فاز جامد ساخته شده توسط یک بستر بسته توسط جریان مایع گسترش مییابد و به حالت متخلخل تغییر میکند. مولکولهای هدف به ذرات بستر متصل شده و ناخالصیها از آن عبور میکنند. این تکنیک نیازی به پیشتصفیه (سانتریفیوژ و فیلتراسیون) ندارد و کارایی بالایی دارد.
تکنیک کروماتوگرافی مسطح (chromatography Planar)
تکنیک کروماتوگرافی مسطح یک روش جداسازی است که در آن فاز ساکن بهصورت یک صفحه وجود دارد. این صفحه میتواند یک کاغذ (در کروماتوگرافی کاغذی) یا لایهای از ذرات جامد که بر روی تکیهگاهی مانند صفحه شیشهای پخش شدهاند (در کروماتوگرافی لایهنازک) باشد.
تکنیک کروماتوگرافی کاغذی (Paper chromatography)
تکنیک کروماتوگرافی کاغذی یک روش است که شامل قراردادن یک نقطه کوچک از محلول نمونه بر روی یک نوار کاغذ کروماتوگرافی میباشد. در این روش، کاغذ در یک شیشه حاوی یک لایه نازک از حلال قرار داده شده و آماده میشود. هنگامی که حلال از کاغذ بالا میرود، با مخلوط نمونه برخورد کرده و شروع به حرکت با حلال میکند. ترکیبات مختلف در مخلوط نمونه بر اساس تعامل آنها با کاغذ، مسافتهای مختلفی را طی میکنند که امکان محاسبه مقدار Rf را فراهم میکند. این مقدار میتواند با ترکیبات استاندارد مقایسه شود تا به شناسایی مادهای ناشناخته کمک شود.
تکنیک کروماتوگرافی لایهنازک (Thin layer chromatography)
تکنیک کروماتوگرافی لایهنازک (TLC) یک روش آزمایشگاهی پرکاربرد است و شبیه تکنیک کروماتوگرافی کاغذی است. بااینحال، بهجای استفاده از یک فاز ثابت کاغذی، شامل یک فاز ثابت از یک لایهنازک جاذب مانند سیلیکاژل، آلومینا یا سلولز بر روی یک بستر صاف و بیاثر است. در مقایسه با کاغذ، مزیت اجرای سریعتر، جداسازی بهتر و انتخاب بین جاذبهای مختلف را دارد. ترکیبات مختلف در مخلوط نمونه باتوجهبه شدت تعامل آنها با جاذب، فواصل مختلفی را طی میکنند و این عامل امکان محاسبه مقدار Rf را فراهم کرده و میتواند با ترکیبات استاندارد برای کمک به شناسایی یک ماده ناشناخته مقایسه شود.
تکنیکها بر اساس وضعیت فیزیکی فاز متحرک (Techniques by physical state of mobile phase)
تکنیک کروماتوگرافی گازی (Gas chromatography)
تکنیک کروماتوگرافی گازی (GC)، همچنین گاهی اوقات بهعنوان کروماتوگرافی گازی مایع، (GLC) شناخته میشود، یک روش جداسازی است که در آن فاز متحرک یک گاز است. کروماتوگرافی گازی همیشه در یک ستون انجام میشود که به طور معمول “بستهبندی شده” یا “مویرگی (capillary)” است.
تکنیک کروماتوگرافی گازی بر اساس تعادل تقسیم آنالیت بین یک فاز ثابت جامد (اغلب یک ماده مبتنی بر سیلیکون مایع) و یک گاز متحرک (اغلب هلیوم) است. فاز ثابت به داخل یک لوله شیشهای با قطر کوچک (یک ستون موئین) یا یک ماتریس جامد در داخل یک لوله فلزی بزرگتر چسبیده است.
این تکنیک به طور گستردهای در شیمی تجزیه استفاده میشود. دماهای بالای استفاده شده در GC آن را برای بیوپلیمرها یا پروتئینهای با وزن مولکولی بالا نامناسب میکند (گرما ساختار آنها را دچار مشکل میکند)، که اغلب در بیوشیمی با آن مواجه میشوند. اما این روش برای استفاده در زمینههای پتروشیمی، نظارت بر محیطزیست و زمینههای شیمیایی صنعتی مناسب است. همچنین به طور گسترده در تحقیقات شیمی استفاده میشود.
تکنیک کروماتوگرافی مایع (Liquid chromatography)
تکنیک کروماتوگرافی مایع (LC) یک تکنیک جداسازی است که در آن فاز متحرک مایع است. کروماتوگرافی مایع را میتوان در یک ستون یا یک صفحه انجام داد. کروماتوگرافی مایع امروزی که معمولاً از ذرات بستهبندی بسیار کوچک و فشار نسبتاً بالا استفاده میکند، تکنیک کروماتوگرافی مایع با کارایی بالا (HPLC) نامیده میشود.
در روش HPLC، نمونه از طریق ستونی که با ذرات نامنظم یا کروی شکل یا یک لایه یکپارچه متخلخل (فاز ثابت) توسط یک مایع (فاز متحرک) در فشار بالا پر شده است، وارد میشود. HPLC بر اساس قطبیت فازهای متحرک و ثابت به دو زیر کلاس مختلف تقسیم میشود.
تکنیکی که در آن فاز ساکن قطبیتر از فاز متحرک است (بهعنوان مثال تولوئن بهعنوان فاز متحرک، سیلیس بهعنوان فاز ساکن) کروماتوگرافی مایع فاز نرمال (NPLC) و برعکس (مثلاً مخلوط آب و متانول بهعنوان فاز متحرک و C18 = اوکتادسیلسیلیل بهعنوان فاز ساکن) کروماتوگرافی مایع فاز معکوس (RPLC) نامیده میشود. از قضا “فاز نرمال” کاربردهای کمتری دارد و بنابراین RPLC به میزان قابل توجهی بیشتر مورد استفاده قرار میگیرد.
تکنیکهای خاصی که تحت این عنوان گسترده قرار میگیرند در زیر فهرست شدهاند. همچنین لازم به ذکر است، درصورتیکه فشاری برای هدایت فاز متحرک در فاز ساکن استفاده نشود، تکنیکهای زیر را میتوان تکنیک کروماتوگرافی مایع پروتئینی سریع در نظر گرفت.
تکنیک کروماتوگرافی سیال فوقبحرانی (Supercritical fluid chromatography)
تکنیک کروماتوگرافی سیال فوقبحرانی یک تکنیک جداسازی است که در آن فاز متحرک سیالی نسبتاً نزدیک به دما و فشار بحرانی آن است.
تکنیکهای مکانیزم جداسازی (Techniques by separation mechanism)
تکنیکهای جداسازی بر اساس مکانیزم جداسازی به روشهای مختلفی دستهبندی میشوند. برخی از این روشها عبارتاند از:
تکنیک کروماتوگرافی تبادل یونی (Ion exchange chromatography)
تکنیک کروماتوگرافی تبادل یونی از مکانیسم تبادل یون برای جداسازی آنالیتها استفاده میکند. معمولاً در ستونها انجام میشود، اما میتوان از مکانیسم آن در حالت مسطح نیز بهره برد. کروماتوگرافی تبادل یونی از یک فاز ثابت باردار برای جداسازی ترکیبات باردار از جمله اسیدهای آمینه، پپتیدها و پروتئینها استفاده میکند. در روشهای مرسوم، فاز ثابت یک رزین تبادل یونی بوده که حامل گروههای عاملی باردار است که با گروههای دارای بار مخالف ترکیبی که باید حفظ شود، تعامل دارند. کروماتوگرافی تبادل یونی معمولاً برای خالصسازی پروتئینها با استفاده از FPLC، که در ادامه توضیح داده خواهد شد، استفاده میشود.
تکنیک کروماتوگرافی حذف اندازه (Size exclusion chromatography)
تکنیک کروماتوگرافی حذف اندازه (SEC) همچنین بهعنوان کروماتوگرافی نفوذ ژل (GPC) یا کروماتوگرافی ژل فیلتراسیون شناخته میشود و مولکولها را بر اساس اندازه آنها (به طور دقیقتر باتوجهبه قطر هیدرودینامیک یا حجم هیدرودینامیک آنها) جدا میکند.
مولکولهای کوچکتر قادر به ورود به منافذ محیط بوده و بنابراین، شستشو طولانیتر میگردد، در حالی که مولکولهای بزرگتر از منافذ حذف میشوند و سریعتر شسته میشوند. به طور کلی یک تکنیک کروماتوگرافی با وضوح پایین بوده و بنابراین اغلب برای مرحله نهایی، “پولیش کردن (polishing)” یک تصفیه اختصاص داده میشود. همچنین برای تعیین ساختار سوم و چهارم پروتئینهای خالص شده مفید است، بهخصوص که میتوان آن را در شرایط محلول طبیعی انجام داد.
تکنیکهای خاص (Special techniques)
تکنیک کروماتوگرافی فاز معکوس (Reversed- phase chromatography)
تکنیک کروماتوگرافی فاز معکوس یک روش شستشو بوده که در کروماتوگرافی مایع استفاده میشود و در آن فاز متحرک به طور قابل توجهی قطبیتر از فاز ساکن است.
تکنیک کروماتوگرافی دوبعدی (Two-dimensional chromatography)
در برخی موارد، یک ستون معین برای جداسازی برخی از آنالیتها کافی نیست. این امکان وجود دارد که یک سری از پیکهای حل نشده بر روی یک ستون دوم با خواص فیزیکی و شیمیایی مختلف (طبقهبندی شیمیایی) هدایت شوند. از آنجایی که مکانیسم نگهداری روی این تکیهگاه جامد جدید با جداسازی اول متفاوت است، میتوان ترکیباتی را که با کروماتوگرافی تکبعدی قابلتشخیص نیستند، جدا کرد.
تکنیک کروماتوگرافی مایع پروتئینی سریع (Fast protein liquid chromatography)
تکنیک کروماتوگرافی مایع پروتئین سریع (FPLC) اصطلاحی است که به چندین تکنیک کروماتوگرافی که برای خالصسازی پروتئینها استفاده میشود، اطلاق میگردد. بسیاری از این تکنیکها مشابه روشهایی هستند که تحت کروماتوگرافی مایع با کارایی بالا انجام میشوند.
تکنیک کروماتوگرافی ضد جریان (Countercurrent chromatography)
تکنیک کروماتوگرافی ضد جریان (CCC) نوعی کروماتوگرافی مایع – مایع است که در آن هر دوفاز ساکن و متحرک مایع هستند. این تکنیک شامل مخلوطکردن محلولی از مایعات است که به آنها اجازه میدهد در لایهها تهنشین شوند و سپس لایهها را جدا میکنند.
تکنیک کروماتوگرافی کایرال (Chiral chromatography)
تکنیک کروماتوگرافی کایرال شامل جداسازی استریوآیزومرها است، بهخصوص انانتیومرها که هیچ تفاوت شیمیایی یا فیزیکی به جز تصاویر آینهای سهبعدی ندارند. این ویژگی باعث میشود که کروماتوگرافی معمولی یا فرایندهای دیگر جداسازی نتوانند انانتیومرها را جدا کنند. برای اینکه جداسازی کایرال انجام شود، فاز متحرک یا فاز ثابت باید بهصورت کایرال شود و تمایلات مختلفی بین آنالیتها ایجاد کند.
ستونهای کروماتوگرافی کایرال با فاز ثابت کایرال در هر دو فاز عادی و معکوس بهصورت تجاری در دسترس هستند، بهطوریکه این تکنیک به انتخاب و جداسازی انانتیومرها بر اساس ویژگیهای کایرال آنها از یکدیگر اجازه میدهد.
جمعبندی
همانطور که اشاره شد، تکنیک کروماتوگرافی، یک روش حیاتی برای جداسازی اجزای مختلف یک ترکیب است. این فرایند شامل استفاده از یک فاز ثابت و یک فاز متحرک است که آنالیت یا مخلوط موردنظر، حل شده در فاز متحرک، بهوسیله نیروی جاذبه یا فشار، از فاز ثابت عبور میکند. اجزای مختلف آنالیت بر اساس ترازمایی به فاز ثابت و انحلالپذیری در حلال، از یکدیگر جدا میشوند. انواع مختلفی از کروماتوگرافی برای هر مطالعه باتوجهبه هدف خاص آن انتخاب و استفاده میشود.