اپی ژنتیک | چیستی، انواع، وراثت و ارتباط آن با سلامت
آیا تا به حال فکر کردهاید که چرا دو قلوهای همسان که از نظر ژنتیکی یکسان هستند، میتوانند از نظر شخصیتی و حتی بیماریهایی که به آنها مبتلا میشوند، تفاوتهای چشمگیری داشته باشند؟ پاسخ این سوال ممکن است در مفهومی به نام اپی ژنتیک نهفته باشد. این مفهوم به ما نشان میدهد که چگونه محیط اطراف ما و تجربیات زندگیمان میتوانند بر نحوه خوانده شدن ژنهای ما تأثیر بگذارند و در نتیجه بر ویژگیهای فیزیکی و روانی ما تأثیر بگذارند. اپی ژنتیک میتواند ژنها را فعال یا غیرفعال کرده و به شیوههای گوناگونی بر سلامت فرد تأثیر بگذارد. با افزایش سن و همچنین قرارگرفتن در معرض عوامل محیطی، الگوهای اپی ژنتیک دستخوش تغییر میشوند. برای آشنایی بیشتر با مبحث اپی ژنتیک، با مجله بیوزوم همراه باشید.
ژنها تأثیر زیادی بر سلامتی افراد دارند، اما رفتارها، محیط (شامل تغذیه و سبک زندگی) و میزان فعالیت بدنی نیز نقش اساسی ایفا میکنند. اپی ژنتیک به مطالعه این موضوع میپردازد که چگونه رفتارها و عوامل محیطی میتوانند تغییراتی ایجاد کنند که بر عملکرد ژنها تأثیر بگذارد. بر خلاف تغییرات ژنتیکی (جهش)، تغییرات اپی ژنتیک قابلبازگشت هستند و توالی بازهای DNA را تغییر نمیدهند، بلکه نحوه خواندن و تفسیر توالی DNA توسط بدن را تحتتأثیر قرار میدهند.
بیان ژن به فرایند تولید پروتئین بر اساس دستورالعملهای ژنها اشاره دارد. هر فرد دارای DNA است که شامل تعداد زیادی ژن میباشد و هر ژن به طور خاصی دستورالعملهایی برای ساخت پروتئین ارائه میدهد. علاوه بر ژنها، DNA شامل بخشهای دیگری است که به طور مستقیم به ساخت پروتئین مربوط نمیشود، اما برای تنظیم و اطمینان از عملکرد صحیح ژنها حیاتی است. این بخشهای اضافی DNA مشخص میکنند که پروتئینها در چه مکان، زمان و میزان تولید شوند.
درحالیکه تغییرات در ژنها (جهش) میتواند پروتئین ساخته شده را تغییر دهد، تغییرات اپی ژنتیکی بر بیان ژن تأثیر میگذارد تا ژنها را روشن یا خاموش کند. این امر میتواند به این معنی باشد که ژنها در سلولها و بافتها، در جایی یا زمانی که به طور معمول این کار را نمیکنند، پروتئین میسازند، یا اینکه ژنها، در جایی و زمانی که به طور معمول این کار را انجام میدهند، پروتئینها را نمیسازند. همچنین میتواند به این معنا باشد که ژنها بیشتر یا کمتر از حد معمول پروتئین میسازند.
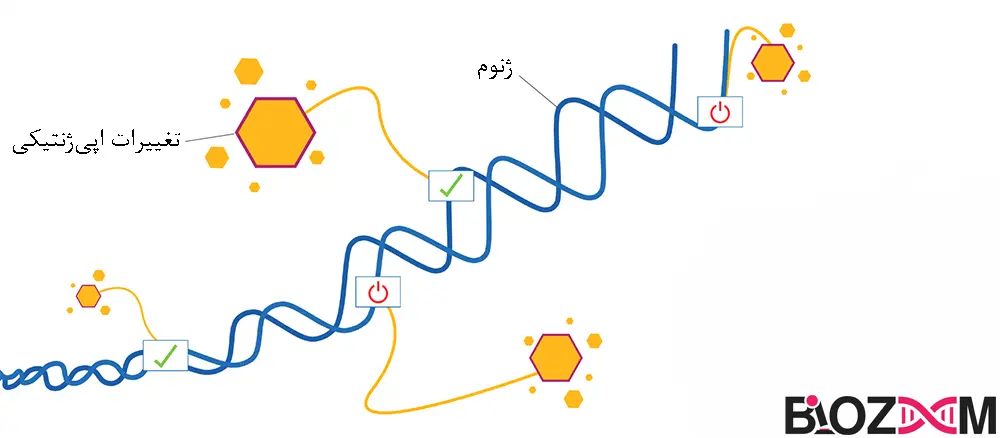
راههای مختلفی وجود دارد که یک عامل محیطی بتواند باعث ایجاد تغییر اپی ژنتیک شود. یکی از رایجترین راهها، ایجاد تغییر در متیلاسیون DNA است. متیلاسیون DNA با افزودن یک ماده شیمیایی (معروف به گروه متیل) به DNA عمل میکند. این ماده شیمیایی همچنین میتواند از طریق فرایندی به نام دیمتیلاسیون از DNA حذف شود. به طور معمول، متیلاسیون، ژنها را خاموش کرده و دیمتیلاسیون ژنها را روشن میکند؛ بنابراین، عوامل محیطی میتوانند بر میزان پروتئینی که یک سلول میسازد تأثیر بگذارند. اگر یک عامل محیطی باعث افزایش متیلاسیون DNA شود، ممکن است پروتئین کمتری ساخته شده و اگر عاملی باعث افزایش دمتیلاسیون شود، ممکن است پروتئین بیشتری ساخته شود.
متیلاسیون DNA
متیلاسیون DNA یک فرایند شیمیایی است که یک گروه متیل را به DNA اضافه میکند. این فرایند بسیار اختصاصی بوده و همیشه در منطقهای اتفاق میافتد که در آن یک نوکلئوتید سیتوزین در کنار یک نوکلئوتید گوانین قرار دارد که توسط یک فسفات به هم متصل شدهاند. این مکان یک سایت CpG نامیده میشود. سایتهای CpG توسط یکی از سه آنزیمی که DNA متیل ترانسفرازها (DNMTs) مینامند، متیله میشوند.
قرارگیری گروههای متیل و پیوستن آن به DNA، ظاهر و ساختار DNA را تغییر داده و برهمکنشهای ژن را با ماشینآلات درون هستهی سلول که برای رونویسی موردنیاز است، تغییر میدهد. متیلاسیون DNA در برخی از ژنها برای تشخیص اینکه کدام نسخه ژنی از پدر و کدام نسخه ژنی از مادر به ارث برده شده است، استفاده میشود، پدیدهای که بهعنوان نشانهگذاری (imprinting) شناخته میشود.
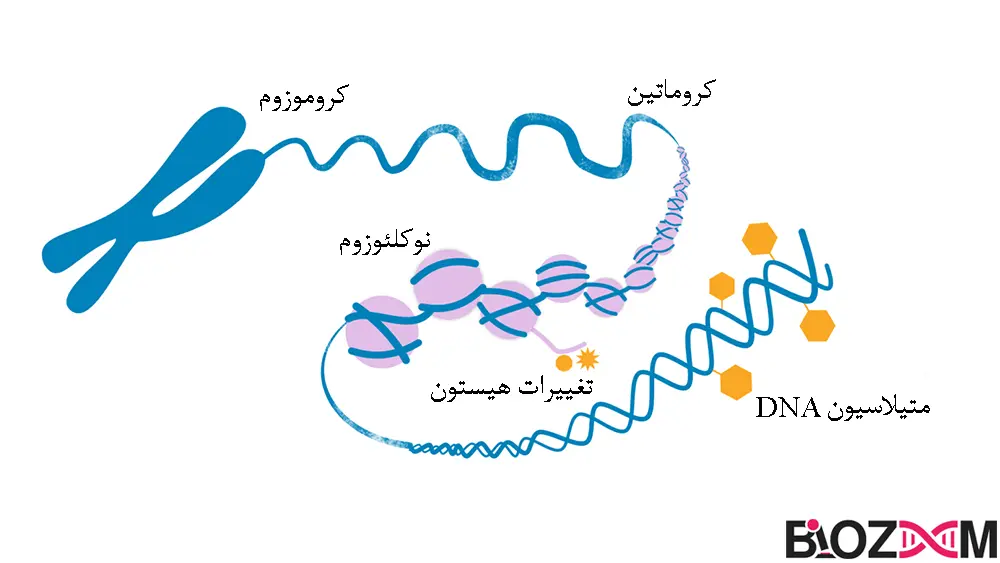
تغییرات هیستون
هیستونهای پروتئینی، اجزای اصلی کروماتین هستند، مجموعهای از DNA و پروتئینها که کروموزومها را میسازند. هیستونها بهعنوان قرقرهای عمل میکنند که DNA میتواند بهدور آن بپیچد. هنگامی که هیستونها پس از ترجمه به پروتئین، تغییر میکنند (تغییر پس از ترجمه)، میتوانند بر نحوه بازآرایی کروماتین تأثیر بگذارند که به نوبه خود میتواند تعیین کند که آیا DNA کروموزومی مرتبط رونویسی خواهد شد یا خیر. اگر کروماتین به شکل فشرده نباشد، فعال است و میتواند DNA مرتبط را رونویسی کند. برعکس، اگر کروماتین متراکم شود (با ایجاد مجموعهای به نام هتروکروماتین)، غیرفعال شده و رونویسی DNA رخ نمیدهد.
دو روش اصلی برای تغییر هیستونها وجود دارد:
- استیلاسیون (Acetylation)
- متیلاسیون (Methylation)
استیلاسیون و متیلاسیون فرایندهای شیمیایی هستند که به ترتیب یک گروه استیل یا متیل را به اسیدآمینه لیزین (Lysine) که در هیستون قرار دارد اضافه میکنند. استیلاسیون معمولاً با کروماتین فعال مرتبط بوده، درحالیکه دیاستیلاسیون بهطورکلی با هتروکروماتین مرتبط است. از سوی دیگر، متیلاسیون هیستون میتواند نشانگری برای هر دو ناحیه فعال و غیرفعال کروماتین باشد. بهعنوان مثال، متیلاسیون یک لیزین خاص (K9) روی یک هیستون خاص (H3) که DNA خاموش را نشان میدهد، به طور گسترده در سراسر هتروکروماتین توزیع شده است. این نوع تغییر اپی ژنتیکی است که مسئول کروموزوم X غیرفعال زنانه است. در مقابل، متیلاسیون یک لیزین متفاوت (K4) روی همان هیستون (H3) نشانگر ژنهای فعال است.
خاموشی مرتبط با RNA
ژنها میتوانند توسط انواع خاصی از RNA غیرفعال شوند. این RNAها میتوانند به سه شکل باشند:
- رونوشتهای آنتیسنس (Antisense RNA): این نوع RNA به رشتهای از ژن که در حال تولید پروتئین است، متصل میشود و مانع از ادامه فرایند تولید پروتئین میگردد.
- RNAهای غیرکدکننده: این RNAها پروتئین تولید نمیکنند، اما میتوانند عملکردهای دیگری داشته باشند که در نهایت بیان ژن را تحتتأثیر قرار میدهند.
- RNA مداخلهگر (RNA interference): این فرایند شامل RNAهایی است که میتوانند باعث تخریب RNA پیامرسان شوند، یعنی همان RNA که دستورالعملهای ساخت پروتئین را حمل میکند، و به این ترتیب از تولید پروتئین جلوگیری میکنند.
این RNAها میتوانند از طریق دو مکانیسم بر بیان ژنها تأثیر بگذارند:
- ایجاد هتروکروماتین: هتروکروماتین بخشی از DNA است که بهشدت فشرده شده و در نتیجه ژنهای موجود در آن خاموش میشوند و پروتئین تولید نمیکنند.
- تغییرات در هیستونها و متیلاسیون DNA: هیستونها پروتئینهایی هستند که DNA بهدور آنها پیچیده شده است. تغییرات در این پروتئینها یا افزودن گروههای شیمیایی به DNA (متیلاسیون) میتواند ژنها را خاموش یا روشن کند.
به زبان سادهتر، RNA میتواند با این روشها جلوی فعالیت یک ژن را بگیرد و تعیین کند که آیا یک ژن فعال باشد یا نه.
تکنیکهای مطالعه اپی ژنتیک
طیف وسیعی از تکنیکهای زیستی برای درک بهتر پدیدههای اپی ژنتیکی در تحقیقات استفاده میشوند:
- استفاده از روشهای بیوانفورماتیکی در محاسبات اپی ژنتیکی
- آنزیمهای محدودکننده حساس به متیلاسیون
- تکنیک نشانهگذاری فلورسنت
- رسوب کروماتین (همراه با انواع مختلف آن Chip-on-chip و ChIP-Seq)
- شناسایی DNA آدنین متیل ترانسفراز (DamID)
- تعیین توالی بیسولفیت
اپی ژنتیک مولکولی
تغییرات اپی ژنتیکی بدون تغییر در توالی ژنتیکی DNA، نحوه فعالشدن ژنهای خاص را تغییر میدهند. این تغییرات ممکن است شامل اصلاح پروتئینهای مرتبط با کروماتین یا ساختار DNA باشد که میتواند منجر به فعال یا غیرفعالشدن ژنها شود. این مکانیسم به سلولهای تمایزیافته در موجودات چندسلولی اجازه میدهد تا فقط ژنهای مورد نیاز خود را فعال کنند. بیشتر این تغییرات اپی ژنتیکی تنها در طول زندگی یک موجود زنده خاص اتفاق میافتند.
بااینحال، تغییرات اپی ژنتیکی میتوانند از طریق فرایندی به نام وراثت اپی ژنتیک تراریخته، به فرزندان ارگانیسم انتقال یابند. علاوه بر این، اگر غیرفعالشدن ژن در سلول تخمک یا اسپرم منجر به لقاح شود، این تغییر اپی ژنتیکی نیز میتواند به نسل بعدی منتقل شود.
فرایندهای خاص اپی ژنتیکی موارد زیر را شامل میشوند:
- پاراموتاسیون (Paramutation)
- نشانهگذاری
- نقشپذیری ژنی (Genomic imprinting)
- خاموششدن ژن (Gene silencing)
- غیرفعالسازی کروموزوم X (X chromosome inactivation)
- اثر موقعیت
- برنامهریزی مجدد متیلاسیون DNA (Reprogramming of DNA methylation)
- ترانسفورماتور (Transformator)
- اثرات سلول مادری، پیشرفت سرطان
- بسیاری از اثرات تراتوژنها (Teratogene)
- تنظیم تغییرات هیستون و هتروکروماتین
ارتباط اپی ژنتیک و سلامت چیست؟
اپی ژنتیک ممکن است نقش مهمتری از ژنتیک در بروز بسیاری از بیماریها داشته باشد. این حوزه از علم با بررسی تغییرات در بیان ژنها بدون تغییر در توالی DNA، بینشهای جدیدی در مورد علل بیماریها ارائه میدهد. اپی ژنتیک کاربردهای پزشکی بالقوه گستردهای دارد که شامل مکانیسمهای پیری، رشد و تکامل انسان، و همچنین ریشههای بسیاری از بیماریها مانند سرطان، اختلالات روانی، بیماریهای قلبی و عروقی و بسیاری دیگر است. این تحقیقات میتواند به توسعه روشهای درمانی جدید و شخصیسازیشده کمک کند، که بهجای تمرکز صرف بر ژنها، تغییرات اپی ژنتیکی را نیز هدف قرار میدهند.
آیا اپی ژنتیک به ارث میرسد؟
اپی ژنتیک، که وظیفهی نظارت بر فعال یا غیرفعال بودن ژنهای خاص در بدن را بر عهده دارد، تأثیرات عمیقی بر سلامت و رشد فرد دارد. این فرایند حتی میتواند بر تمایل به ابتلا به سرطان، چاقی یا لاغری تأثیر بگذارد. وراثت اپی ژنتیک و انتقال الگوهای بیان ژن از نسلی به نسل دیگر، به یکی از موضوعات جذاب و پرمخاطب در تحقیقات علمی تبدیل شده است. این مفهوم که تغییرات اپی ژنتیکی میتوانند از والدین به فرزندان و حتی نوهها منتقل شوند، زمینهساز کشفیات جدیدی در علم ژنتیک شده است.
محققان توضیح میدهند که هر سلول در بدن انسان دارای DNA یکسانی است، اما نحوه بیان ژنها در هر مرحله از زندگی توسط اپی ژنتیک تعیین میشود. برای مثال، در طول رشد، نشانگرهای اپی ژنتیکی فرایند تمایز را کنترل میکنند؛ این تمایز باعث میشود یک سلول ماهیچهای با فعالکردن ژنهای خاص، متفاوت از یک سلول کلیوی شود و این الگو به نسلهای بعدی سلولها منتقل میشود، بهطوری که سلول ماهیچهای همیشه ماهیچه و سلول کلیوی همیشه کلیه باقی میماند.
در پروانه سلطنتی، مراحل مختلف زندگی مانند کرم ابریشم، پیله و پروانه، همگی فنوتیپهای متفاوتی از یک DNA یکسان هستند که تحت کنترل اپی ژنتیک قرار دارند. نکته جالبتوجه این است که این کنترلها میتوانند تغییر کنند. عواملی مانند رژیم غذایی، وضعیت روانی، قرارگرفتن در معرض دود سیگار، ورزش، وضعیت مالی و سایر عوامل محیطی یا سبک زندگی میتوانند بر بیان ژنها تأثیر گذاشته و آنها را فعال یا غیرفعال کنند.
تحقیقاتی که اخیراً در مجلات علمی مانند Cell، Nature و Nature Genetics منتشر شده نشان میدهند که اطلاعات اپی ژنتیکی میتوانند از نسلی به نسل دیگر منتقل شوند؛ اما ممکن است این فرضیه نادرست نیز باشد. مادربزرگی که سیگار میکشد، اپی ژنوم خود را تغییر میدهد و در تئوری میتواند پیکربندی اپی ژنتیکی مضر ناشی از عادت خود را منتقل کند. تحقیقات نشان داده که سیگارکشیدن میتواند باعث افزایش غیرطبیعی هورمونهایی شود که سیگنال گرسنگی را نشان میدهند و اگر این امر ارثی باشد، میتواند منجر به چاقی در نوهاش شود.
آیا علم تأیید کرده است که تأثیرات اپی ژنتیکی میتوانند به نسلهای بعدی منتقل شوند؟
ابتدا باید بدانیم که تکامل بهطورکلی در برابر وراثت اپی ژنتیکی مقاومت میکند. تغییرات اپی ژنتیکی از طریق سه مکانیسم مختلف رخ میدهند که متیلاسیون DNA بیشترین توجه را به خود جلب کرده است. در این فرایند، گروههای متیل، که از اتمهای مشتق شده از متان تشکیل شدهاند، به مولکولهای DNA متصل میشوند و تعیین میکنند که کدام ژنها باید فعال یا غیرفعال باشند. اما در طول تولیدمثل، سلولهای پستانداران دو چرخه کامل از دمتیلاسیون را تجربه میکنند که در این فرایند، تمامی گروههای متیل و در نتیجه، اطلاعات اپی ژنتیکی از سلولهای زایا و جنینی حذف میشود. تاکنون، هیچ مدرکی وجود ندارد که نشان دهد اطلاعات اپی ژنتیکی میتواند از دو دور این پاکسازی بیوشیمیایی جان سالم به در ببرد.
دوم، برای اثبات اینکه یک تغییر اپی ژنتیکی میتواند به نسلهای بعدی منتقل شود، باید اطمینان حاصل کرد که هرگونه اثر مشاهده شده ناشی از قرارگرفتن در معرض محیط در رحم نباشد. برای مثال، اگر یک موش باردار آگوتی با خز زردرنگ از رژیم غذایی غنی از گروههای متیلدهنده (یک رژیم غذایی سالم) تغذیه شود، فرزندانی عمدتاً سالم با پوشش قهوهای به دنیا میآورد. اما اگر از غذای معمولی موش استفاده کند، فرزندانش اغلب چاق، با خز زرد و با سلامت ضعیفتری متولد میشوند. این نمونه به طور واضحی یک اثر اپی ژنتیکی است، اما فرا نسلی نیست؛ زیرا این تغییرات ناشی از تأثیر موقتی یک محرک محیطی، یعنی غذایی است که مادر موش در دوران حساس رشد جنین مصرف میکند.
قرارگرفتن در معرض چنین شرایطی میتواند تغییرات دائمی در متابولیسم و افزایش خطر ابتلا به بیماریهای مزمن ایجاد کند، اما این به معنای انتقال اپی ژنتیکی از مادر به فرزندان نیست. این اثرات بیشتر شبیه به تغییراتی هستند که در لارو زنبورعسل دیده میشود. لاروهایی که با ژل رویال تغذیه میشوند، به ملکههایی بزرگ، با عمر طولانی، بارور و با فعالیت مغزی کمتر تبدیل میشوند. در مقابل، لاروهایی که با ژل کارگری تغذیه میشوند، کوچکتر، با عمر کوتاهتر، اما از نظر عصبی بسیار فعالتر هستند.
ادعاهایی مبنی بر اینکه اپی ژنتیک میتواند بر چندین نسل از خانوادههایی که بنیانگذاران آنها از قحطی یا دیگر رویدادهای آسیبزا جان سالم به در بردهاند تأثیر بگذارد، بهویژه در انسانها، بهسختی قابلاثبات است. برای اینکه چنین تأثیراتی بهعنوان ارثی شناخته شوند، باید حداقل در چهار نسل در خط مادری مشاهده شوند.
دلیل این امر آن است که سلولهای تناسلی زنانه حتی قبل از تولد تشکیل و تثبیت میشوند؛ بنابراین، اگر مادری در دوران بارداری سیگار بکشد، این رفتار نهتنها بر خودش و فرزند متولد نشدهاش تأثیر میگذارد، بلکه اگر آن فرزند دختر باشد، نسل سوم را نیز از طریق سلولهای تولیدمثلی آن دختر تحتتأثیر قرار میدهد.
در مردان، ازآنجاکه اسپرم به طور مداوم در طول زندگی تولید میشود، تنها سه نسل برای اثبات وراثت اپی ژنتیک موردنیاز است، اما حتی این بازه زمانی برای هر محققی که روی انسان مطالعه میکند بسیار طولانی است. حتی در حیوانات آزمایشگاهی، هیچ محققی وراثت اپی ژنتیکی فرا نسلی را ثابت نکرده است. علیرغم ادعاهایی که در معتبرترین مجلات علمی وجود دارد، تا به امروز هر آزمایش را میتوان با مواجهه درون رحمی یا مکانیسمهای دیگر توضیح داد.
یک استثنای خاص وجود دارد که از طریق مکانیسمی پیچیده و هنوز بهطور کامل ناشناخته به نام چاپ ژنومی رخ میدهد. به نظر میرسد این نوع وراثت فرا نسلی محدود به ژنهایی است که نقش مهمی در کنترل رشد جنین دارند. بهطور کلی، آللهای پدری این ژنها فعال هستند و به رشد کمک میکنند، در حالی که آللهای مادری غیرفعال میمانند. این الگوی روشن و خاموش بودن آللها بادقت از نسلی به نسل دیگر منتقل میشود و بهطور مستمر حفظ میگردد.
وراثت اپی ژنتیک ممکن است وجود داشته باشد، اما ثابت نشده و باتوجهبه اپیدمی فعلی رفتارهای کمتحرک و چاقی، شاید مکانیسمهایی که سلولهای تولیدمثلی ما را از حافظه چنین حالتهای تعدیل شده اپی ژنتیکی از نسلی به نسل دیگر محروم میکند، «یک چیز خوب» باشد!
جمعبندی
بهطور خلاصه، اپی ژنتیک به کنترل ژنها از طریق عواملی غیر از تغییرات در توالی DNA اشاره دارد، شامل تأثیرات محیطی و رفتاری. تغییرات اپی ژنتیکی میتوانند ژنها را فعال یا غیرفعال کرده و تعیین کنند که کدام پروتئینها تولید شوند. این تغییرات به توالی DNA خود آسیبی نمیزنند، بلکه بر نحوه خواندن و تفسیر این توالی تأثیر میگذارند و در نتیجه، دستورالعملهای تولید پروتئین را تنظیم میکنند. اپی ژنتیک نقش کلیدی در بسیاری از فرایندهای طبیعی سلولی دارد و بهطور گسترده در تنظیم فعالیتهای ژنی و عملکردهای سلولی دخالت میکند.