مرگ سلولی | چیستی، علل وقوع و انواع
یکی از جنبههای بسیار حیاتی در دستیابی به سلامت و بقای بدن، تنظیم و کنترل مرگ سلولی است. این فرآیند، که به عنوان یکی از جوانب بنیادین زندگی موجودات چندسلولی شناخته میشود، تضمین میکند که سلولها بازسازی و جایگزین شوند تا عملکرد بدن بهینه باقی بماند. همچنین گفتنی است، سلولهایی که به علت استهلاک یا عدم توانایی در انجام وظایفشان، برای بقای بدن مضر محسوب میشوند، از طریق مرگ سلولی از بین میروند. این فرآیند به عنوان یک سیستم تنظیمشده و کنترلشده، طی فعالیتهای متعددی مانند آپوپتوز و اتوفاژی، به صورت برنامهریزیشده اتفاق میافتد. مرگ سلولی نشان میدهد که بدن همیشه به دنبال بهینهسازی و بهبود است. با از بین رفتن سلولهای قدیمی و ضعیف، جای خالی آنها را سلولهای جدید و قوی تر پر میکنیم، که این امر به بقا و عملکرد بهتر بدن کمک میکند. اما، هنگامی که این فرآیند بهطور نادرست یا ناقص اتفاق میافتد، مشکلاتی نظیر سرطان بروز میکند. در این حالت، سلولها از دست رفته نمیشوند یا سلولهای آسیبدیده ادامه مییابند، که این میتواند به مشکلات جدی سلامتی منجر شود.
بنابراین، درک و کنترل مرگ سلولی یکی از مهمترین عوامل در حفظ سلامت و جلوگیری از بروز بیماریهای مختلف است. از این رو، پژوهشهای بیشتری برای درک عمیقتر این فرآیند و کشف راهکارهایی برای مداخله در آن انجام میشود تا بتوان بهبودی در درمان بیماریها و حفظ سلامتی بیشتری را فراهم کرد.
در ادامه با مجله بیوزوم همراه باشید تا بیشتر با مرگ سلولی و انواع آشنا شویم.
مرگ سلولی زمانی اتفاق میافتد که سلولهای بدن ازکارافتاده و میمیرند. سلولهای بدن طی فرایندی به نام تقسیم سلولی یا میتوز تکثیر میشوند. کارشناسان بر این باورند که سلولهای انسان سالم قبل از مرگ میتوانند تا 60 برابر تکثیر یا تقسیم شوند. بدن به طور مداوم در حال ساخت سلولهای جدید برای جایگزینی سلولهای آسیب دیده و در حال مرگ است.
مرگ سلولی طبیعی بدن را سالم و کارآمد نگه میدارد. مشکلات زمانی به وجود میآیند که مرگ سلولها آنطور که انتظار میرود اتفاق نمیافتد یا سلولها زمانی که نباید میمیرند.
مطلب مرتبط: نگاهی بر انواع سلول ، سازندگان حیات
چه چیزی باعث مرگ سلولی میشود؟
دلایل زیادی برای مرگ سلولها وجود دارد:
- برخی از سلولها در حین رشد، قبل از تشکیل کامل میمیرند.
- سلولهای پیر به سنی میرسند که دیگر توان تقسیم شدن نداشته و میمیرند.
- سلولهای آسیب دیده غیرقابلترمیم به طور طبیعی از بین میروند.
- بیماریها، جراحات، سموم و درمانهای خاص به سلولها آسیب رسانده و باعث مرگ سلولی میشوند.
در ادامه انواع مرگ سلولی که در بدن رخ میدهد را مورد بررسی قرار میدهیم.
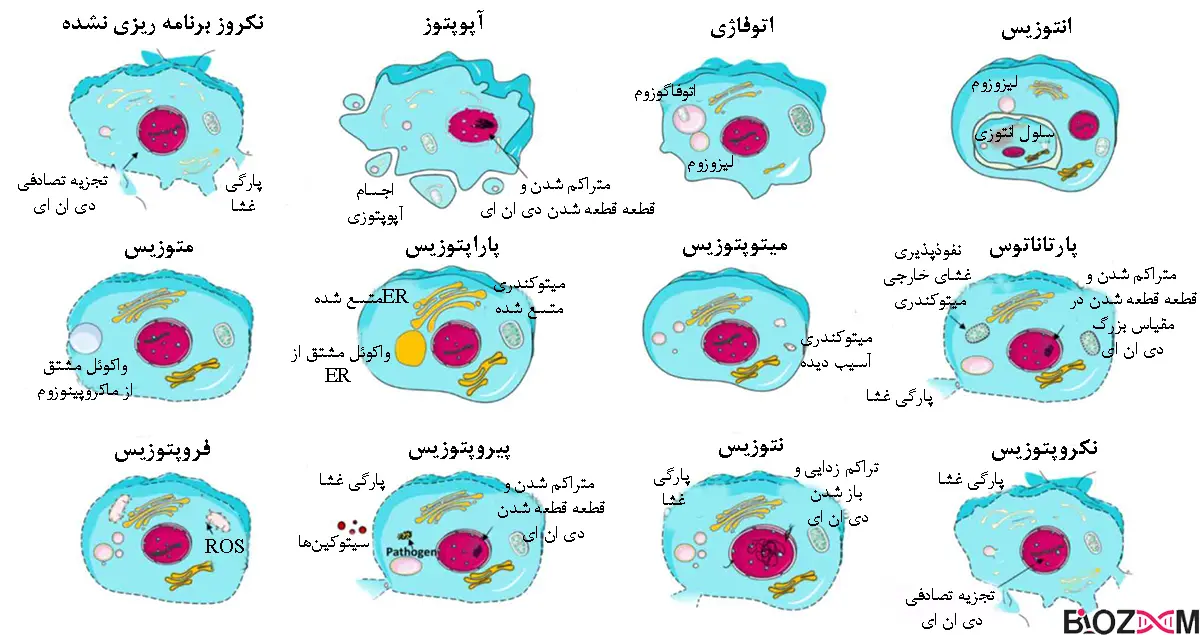
انواع مرگ سلولی
در این بخش از مطلب قصد داریم تا هریک از انواع مرگ سلولی را بیان کرده و درباره آن توضیح دهیم
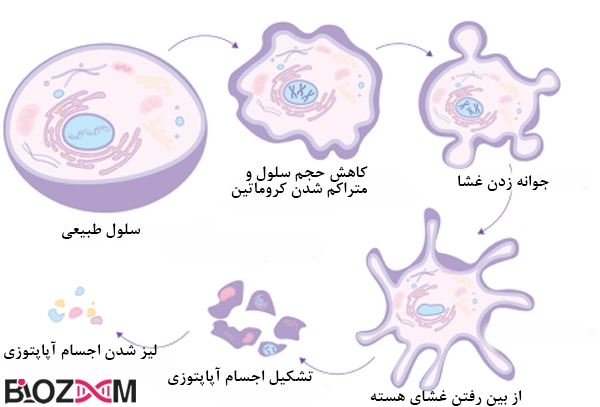
Apoptosisمرگ سلولی برنامه ریزیشده (آپاپتوز یا آپوپتوز)
آپوپتوز، یک مکانیسم مرگ سلولی برنامهریزیشده ضروری، برای از بین بردن سلولهای آسیب دیده یا قدیمی است و در رشد ارگانیسم، هموستاز بافت، و دفاع میزبان در برابر سلولهای آلوده به میکروارگانیسمها نقش دارد.
آپوپتوز در چندین مرحله انجام شده که با تغییرات بارز در مورفولوژی سلول و تغییرات مولکولی ظریفتر مشخص میشود که میتواند در بلعیدهشدن سلولهای آپوپتوزی توسط فاگوسیتهایی مانند ماکروفاژها به اوج خود برسد.
دو مسیر آپوپتوز متفاوت وجود دارد:
- مسیر داخلی
- مسیر خارجی
مسیر داخلی با واسطه میتوکندری در پاسخ به محرکهای داخلی مانند آسیب DNA رخداده و در آن کاسپازهای اعدام (executioner caspases)، عمدتاً کاسپاز-3 دخیل هستند.
مسیر بیرونی با اختلال در ریزمحیط خارج سلولی که توسط گیرندههای غشای پلاسمایی شناسایی میشود، توسط کاسپاز-8 و با واسطه گیرندههای مرگ خارج سلولی (بهعنوان مثال، اتصال FasL به CD95) آغاز میشود.
مرگ سلولی خودخواری یا اتوفاژی (Autophagy)
اتوفاژی یک فرایند فیزیولوژیکی است که بهصورت انتخابی یا غیرانتخابی، هموستاز را با تخریب پروتئین و تغییر اندامکهای سلولی آسیب دیده برای تشکیل سلول جدید حفظ میکند. بااینحال، مرگ سلولی وابسته به اتوفاژی ممکن است تحت شرایط خاصی رخ دهد. سه نوع اصلی اتوفاژی وجود دارد:
- ماکرو اتوفاژی: محتوای سیتوپلاسمی از طریق ادغام با اتوفاگوزوم به لیزوزوم تحویل داده شده تا یک اتولیزوزوم تشکیل شود.
- میکرو اتوفاژی: محتوای سیتوپلاسمی توسط هجوم غشای لیزوزوم بلعیده میشود.
- اتوفاژی با واسطه چاپرون: پروتئینهای هدف که در غشای لیزوزوم بهصورت کمپلکس با پروتئینهای چاپرون حمل میشوند، پس از شناسایی توسط گیرنده غشای لیزوزومی، پروتئین غشایی 2A مرتبط با لیزوزوم (LAMP-2A)، تخریب میشوند.
ماشین اتوفاژیک فرایند پیچیدهای است. اما اساساً شامل پنج مرحله است:
- تشکیل فاگوفور توسط سیگنالهای استرس.
- شروع تشکیل اتوفاگوزوم.
- گسترش اتوفاگوزومی و گرفتن مولکولهای هدف برای تجزیه.
- تکمیل اتوفاگوزوم.
- اتوفاگوزوم با لیزوزوم ترکیب میشود و تخریب پروتئولیتیک مولکولهای بلعیده شده اتوفاگوزوم، توسط آنزیمهای لیزوزوم، انجام میشود
مرگ انتوتیک Entotic cell death
مرگ سلولی انتوتیک یا انتوزیس، فرایندی است که سلولها را هدف قرار میدهد تا پس از بلعیدهشدن توسط سلولهای مجاور، توسط درونیسازی سلول در سلول وابسته به اکتومیوزین (actomyosin-dependent cell-in-cell internalization) از بین بروند. مرگ سلولی انتوتیک با بلعیده شدن سلولها از طریق هضم لیزوزومی وابسته به پروتئین اتوفاژی اتفاق میافتد.
فروپتوزیز Ferroptosis
فروپتوزیس یک شکل وابسته به آهن و ROS از مرگ برنامهریزیشده است که توسط اختلالات اکسیداتیو ریزمحیط داخل سلولی آغاز میشود. توسط چندین مولکول، بهعنوان مثال گلوتاتیون پراکسیداز (GPX4)، NADPH اکسیداز (NOX)، p53 و فاکتور هستهای E2 مرتبط با فاکتور 2 (NRF2) که به طور مستقیم یا غیرمستقیم متابولیسم آهن و پراکسیداسیون لیپیدی را هدف قرار میدهند، تنظیم میشود.
مرگ سلولی ایمونوژنتیک Immunogenic cell death
مرگ سلولی ایمونوژنیک، فعالشدن یک پاسخ ایمنی در میزبانهای دارای سیستم ایمنی نسبت به محرکهای خاصی مانند آنتیژنهای ویروسی یا سلولی است. این فرایند شامل آزادسازی واسطههای محلول مانند DAMP در حضور این محرکها است. گیرندههای تشخیص الگو در سطح سلولهای پاسخ ایمنی ذاتی و تطبیقی، DAMPها را تشخیص داده و پاسخ ایمنی را ایجاد میکنند.
Lysosome-dependent cell death
آسیب لیزوزومها توسط فعالیت کاتپسین، بهعنوان مثال در نتیجه سموم باکتریایی و ویروسی یا گونههای فعال اکسیژن (ROS)، اغلب منجر به نفوذپذیری غشای لیزوزومی (LMP)، با انتشار محتوای آن از جمله آنزیمهای پروتئولیتیک از خانواده کاتپسینها در داخل سیتوپلاسم میشود. این اتفاقات منجر به فعالشدن مسیرهای سیگنالینگی شده که باعث بروز مرگ برنامهریزیشده سلولی میگردد.
Mitochondrial permeability transition (MPT)-driven necrosis
مرگ نکروز ناشی از انتقال نفوذپذیری میتوکندری، در طول استرس اکسیداتیو (oxidative stress) و از دست دادن نفوذناپذیری غشای داخلی میتوکندری (IMM) ایجاد شده که به دلیل اختلال در ریزمحیط داخل سلولی، منجر به شکست اسمزی غشای میتوکندری و در نتیجه مرگ برنامهریزیشده میشود. سیکلوفیلین D (CYPD) در این فرایند دخیل است.
Mitotic death
مرگ سلولی ناشی از فشارهای فیزیکی و یا شیمیایی است که منجر به القای میتوز میشود. مرگ میتوتیک در مراحل اولیه نکروز و آپوپتوز دیده میشود. این شکل از مرگ برنامهریزیشده که بهعنوان فاجعه میتوتیک نیز شناخته میشود، یک مکانیسم سرکوبکننده سرطان برای کنترل سلولهای ناکارآمد میتوز است.
Necroptosis
نکروز برنامهریزیشده (نکروپتوز) توسط اختلالات هموستاز خارج سلولی یا درونسلولی که معمولاً شامل واسطههایی مانند گیرندههای مرگ و اینترفرون است، القا میشود. RIPK3 و سوبسترای آن MLKL پروتئینهای تعیینکننده حیاتی مسیر نکروپتوز هستند. گمان میرود که اختلال در نکروپتوز با سرطان، بیماریهای التهابی و نورودژنراتیو مرتبط باشد.
NETotic cell death
مطالعات نشان داده که نوتروفیلهای فعال، تلههای خارج سلولی (NETs) را آزاد میکنند که شبکهای را با پروتئینهای ضدمیکروبی متصل تشکیل داده که برای بیحرکت کردن و هم از بین بردن پاتوژنها عمل میکنند. فرایند تشکیل و آزادسازی NET (نتوزیس) منجر به مرگ سلولی برنامهریزیشده نوتروفیل میشود.
Oxeiptosis
یک مسیر مرگ برنامهریزیشده سلولی که شامل پیامرسانهای سیگنالینگ ROS است. تصور میشود که انواع سلولها مانند فیبروبلاستها و سلولهای اپیتلیال به اکسیپتوزیس مرتبط با تجمع ROS حساس هستند، در حالی که لنفوسیتها مقاومتر به نظر میرسند. تجمع ROS و جهش در حسگرهای ROS، مانند KEAP1 که یک مجموعه با NRF2 و PGAM5 تشکیل میدهد، با پیشرفت بیماری و سرطان مرتبط است.
Parthanatos
فعالسازی پلی (ADP-ribose) پلیمراز-1 (PARP-1)، زمانی که تحت استرس اکسیداتیو قرار دارد، منجر به مرگ برنامهریزیشده سلولی توسط پارتاناتوس میشود. ویژگیهای مرگ سلولی توسط پارتاناتوس عبارتاند از تنظیم بیان مثبت PARP-1، تجمع پلیمرهای پلی ADP-ریبوز، دپلاریزاسیون میتوکندری و انتقال هستهای فاکتور القاکننده آپوپتوز (AIF).
Pyroptosis
فعالشدن التهابی کاسپازهای 1 در انسان و 11 در موش (همسان با کاسپاز 4 و 5 در انسان)، منجر به برش گسدرمین D (gasdermin D) میشود که شروع کننده پیروپتوزیس است. دومین N ترمینال گسدرمین D برش خورده به غشای پلاسمایی متصل میشود، منافذ تشکیل شده و اجازه آزاد شدن IL-1بتا و هجوم سدیم و آب را میدهد که منجر به پارگی غشا میشود.
بیماریهای مرگ سلولی
موارد زیر تعدادی از بیماریهایی هستند که به طور کامل یا جزئی به دلیل عدم تعادل در روند مرگ سلولی ایجاد میشوند.
افزایش مرگ سلولی
- بیماری آلزایمر
- بیماری هانتینگتون (Huntington)
- بیماری پارکینسون (Parkinson)
- کمخونی آپلاستیک (Aplastic)
- حمله قلبی
- سکته
- دیابت نوع یک
- اماس (MS)
- ایدز (HIV)
کاهش مرگ سلولی
- سرطان
- آترواسکلروزیس (Atherosclerosis)
- لوپوس اریتماتوز سیستمیک (SLE)
- روماتیسم مفصلی (Rheumatoid arthritis)
- پوکیاستخوان (Osteoporosis)
- سندرم داون(dawn syndrome)
جمعبندی
همانطور که اشاره شد، مرگ سلولی برنامهریزی شده یک فرایند فیزیولوژیک در بدن است که عملکرد سلولهای قدیمی و آسیب دیده را متوقف میکند تا سلولهای جدید و کارآمد جایگزین آنها شوند. انواع مرگ سلولی مانند آپوپتوز، اتوفاژی و نکروپتوزیس در بدن رخ میدهند که هرکدام مسیرهای سیگنالینگ و مکانیسمهای ویژه خود را دارند. هرگونه عدم تعادل در مرگ سلولی یعنی افزایش یا کاهش آن، موجب بیماریهایی از جمله آلزایمر و سرطان میگردد، بنابراین مرگ سلولی طبیعی در حفظ بقا و سلامت بدن بسیار اهمیت دارد.